其他辅助检查:
1.超声检查 腹部超声探查是B-CS应首选的、有价值的、非创伤性检查。在我国,目前已普及到基层医院。
(1)实时超声波检查:腹部B超可对多数病例做出初步正确诊断,其符合率可达95%以上。急性B-CS时肝脏肿大和腹水多是突出的表现。肝静脉阻塞时,可见静脉壁增厚、狭窄、或有血栓形成的回声;若仅为肝静脉出口部阻塞,可见肝内静脉扩张及肝内、外侧支循环出现。慢性型者可多见尾叶增大,这常是B-CS的特征性表现。随病程的延长,肝脏可出现局部硬化、萎缩,而另一叶或伴尾叶增大,但门静脉不像肝内型门静脉高压时扩张明显。脾脏肿大也不如门脉型肝硬化时那样突出,多为轻度或中度肿大。下腔静脉膜性闭锁(MOVC)时,可见下腔静脉肝后段有膜状阻塞,阻塞平面以下,下腔静脉扩张(Ⅰ型)。若下腔静脉肝后段呈长节段狭窄,可见其血管壁增厚,有时伴有血管内、外的瘢痕强回声,而肝静脉出口部可部分或完全阻塞,肝内可有侧支循环形成(Ⅱ型)。当下腔静脉肝后段长节段受阻,其腔内可探及巨型血栓,由于血栓头部机化,其回声远较远端红血栓部分为强。部分病例整个血栓均可为强回声,病程多属长久者(Ⅲa型或Ⅲb型)。此外,B超可以显示肝脏、胆道、肾脏、肾上腺等有无占位病变,有助于了解病因和进行鉴别诊断。同时,可了解有无腹水存在、脾脏有无肿大;对肝外门静脉、肠系膜上静脉及脾静脉探查是否通畅;有无扩张、狭窄及血栓形成。但B超对肝外侧支循环状态的检出难以令人满意,而对血栓的辨识常优于血管造影。
(2)多普勒超声:多普勒超声对B超具有很高的诊断价值。肝、腔静脉的血流信号消失,可以肯定有阻塞存在;肝静脉、门静脉或下腔静脉有逆向血流信号,也可以判断有阻塞。正常的肝静脉血流频谱呈时相性变化,其波形变化随心动周期而改变,其最大和最小血流速度之比常大于4.0。这种时相变化的消失,呈现平流或稳流,则提示下腔静脉或肝静脉出口部的阻塞。此种变化在肝硬化时,约有80%可表现出来。但在B-CS时,下腔静脉中下段可见血液逆流,以资鉴别。Bolondi指出,多普勒诊断B-CS的敏感性为87.5%。此外,多普勒超声还可对下腔静脉、门静脉的通畅情况和血流方向及闭塞轮廓给予清晰显示。
2.肝静脉、下腔静脉、门静脉及动脉造影 血管造影是确立B-CS诊断的最有价值的方法,常用的造影有以下几种:
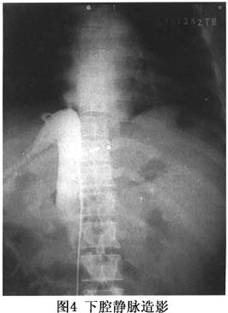
(1)下腔静脉造影:采用Seldinger技术,行股静脉穿刺,经导丝将导管引至下腔静脉肝段,首先测定下腔静脉压(IVCP),此时造影可明确阻塞的程度和部位、局部病变的形态及侧支循环形成情况。必要时,可同时经颈静脉或贵要静脉插管,经上腔静脉、右心房再至下腔静脉上段,作对端造影,更可清晰显示阻塞部位、程度、范围和侧支循环状况。对病变的形态,隔膜的厚度,中央是否有孔或呈筛状,可呈现喷壶嘴征或沙漏征,隔膜附着方式是水平天幕状或斜形僧帽状,有无膜下血栓繁衍,有无附壁血栓等均可有所了解。若肝静脉开口部位于隔膜之下且并无受阻时,在下腔静脉显影的同时,肝静脉亦可显影(图4)。此时,还可见心包膈静脉、腰静脉、膈静脉、腰升静脉及椎前静脉的扩张显影。总之,下腔静脉造影,即便是单向造影,一般情况下,结合临床,可以对B-CS做出诊断,对少数病例,可行对端插管做双向造影。
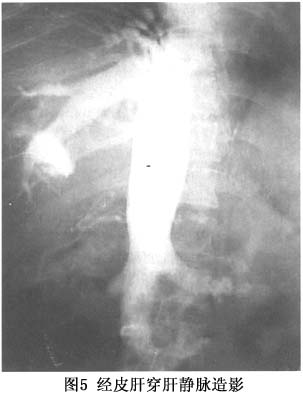
(2)经皮肝穿肝静脉造影(percutaneous transhepatic hepatovenography,PTHV):肝静脉造影对B-CS应是最直接、最清晰的检查方法。但当肝静脉闭塞时,传统的经股静脉插管至下腔静脉,再经肝静脉开口逆行插管造影难以实施。而经皮肝穿肝静脉造影,不仅简便、安全、且成功率高,多数情况下,在肝静脉显影的同时,下腔静脉亦可同时显影(图5)。郑州大学一附院将下腔静脉造影及经皮肝穿肝静脉造影作为诊断B-CS的常规检查项目,除早年的部分病例外,497例手术的病人做了检查,29例造影剂进入包膜下或膈下,468例造影成功,从而对B-CS最终确立了诊断,并明确了分型。近年来的353例,均在电视屏幕明视下造影,成功率达100%。
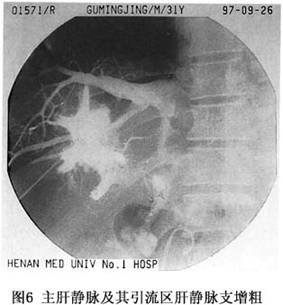
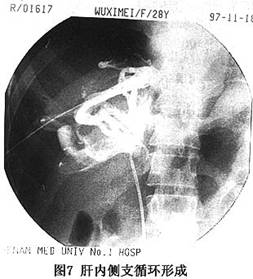
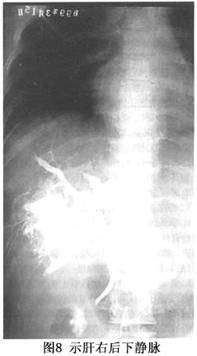
正常肝静脉造影应为棒状或伴有部分分支显影,造影剂经下腔静脉流入右心房。当肝静脉出口部受阻时,可见主肝静脉及其引流区域的肝静脉支增粗(图6)。慢性病例,可见肝内形成侧支循环,出现“蛛网征”(cobweb’sign,图7),如若下腔静脉病变隔膜位于主肝静脉出口部以上,且肝静脉本身未被累及时,可见主肝静脉扩张,下腔静脉亦扩张(图4)。在急性病例,肝静脉可有狭窄、阶段性阻塞,在肝内可见侧支循环形成或与门静脉分支形成短路,此时门静脉干支亦可显影。少数急性或亚急性病例,除肝静脉广泛狭窄外,其出口部阻塞或呈沙漏状,此与肝小静脉阻塞病(venoocclusive disease of the liver,VOD)相当难以鉴别。当主干静脉完全受阻时,造影剂经肝内的侧支循环,再由肝短或肝背静脉在第三肝门部流入下腔静脉,这些静脉数目不一,有时很粗大,特别是肝右后下静脉,直径有时可达2.0cm(图8)。值得强调指出的是不少B-CS病例(如Ⅱ型和Ⅲb型),主肝静脉出口部闭塞,经下腔静脉插管做逆行肝静脉造影,是难以实施的,对这种病例,经皮肝穿肝静脉造影对B-CS的诊断,更有决定性的意义。
(3)经皮脾穿刺门静脉造影 (PTSP):B-CS对病人危害最大的病变,在急性期为肝损害,在慢性期为门静脉高压症,后者导致的消化道出血,更可威胁患者生命。因此,对门静脉高压症的诊断、鉴别诊断、分型、出血的预测及手术方案的拟定,门静脉造影可提供诸多的与之相关的资料。经脾动脉或肠系膜上动脉插管做门静脉间接造影,由于在B-CS时,门静脉成为肝血液的流出道,影像显示多较浅淡。自1983年以来,采用改良的经皮脾穿刺门静脉造影(MPTSP)对伴有脾肿大和消化道出血的B-CS病例进行检查,效果甚为满意。MPTSP具有方法简便、安全、费用低、易推广的优点。
PTSP对B-CS的临床价值:①PTSP显示的图像较间接造影更为清晰,②根据图像的形态、脾静脉、门静脉的直径、侧支形成、血流方向和脾髓压力等,为各型门静脉高压症的诊断、鉴别诊断、分型等提供信息资料。③当脾髓压力显著增高,门静脉有离肝血流(如显示肠系膜下静脉显影)且缺乏肝病征象时,做PTSP又排除肝前性门静脉高压症之后,应再做下腔静脉造影和PTHV,以证实有无下腔静脉和(或)肝静脉阻塞。④为手术方式的选择提供资料:如对B-CSⅡ型和Ⅲb型病例,若不能采用与下腔静脉的门-体分流术而决定行脾静脉-右心房或脾静脉-颈内静脉架桥术时,必须在术前行PTSP,以具体了解脾静脉的口径、通畅情况及脾髓压力等。⑤观察或评价手术效果:对施行保留脾脏的手术,如脾-肺固定术、肠腔C形架桥术、门-腔分流术等,对前者可了解脾、肺之间术后建立的侧支分流情况及术后脾髓压的下降程度;对后二者术后可通过PTSP了解吻合口通畅情况,亦可通过脾髓压评价降压效果等。
(4)动脉造影:部分B-CS病例,动脉造影有一定临床意义。如当肝脏有可疑癌灶,选择性肝动脉造影对其分辨力较高,对B-CS有无并发肝癌有重要意义。在B-CS时,由于肝脏淤血肿大,可见肝动脉伸直及狭窄。在肠系膜上动脉造影时,其静脉相可见门静脉血液逆流及门-奇静脉自然分流影像时,支持B-CS的诊断。
3.CT扫描 在B-CS急性期,CT平扫可见肝脏呈弥漫性低密度肿大且伴有大量腹水。CT扫描的特异性表现是下腔静脉肝后段及主肝静脉内出现高度衰退的充盈缺损(60~70Hu)。增强扫描对B-CS的诊断具有重要意义。注射造影剂后30s,可见肝门附近出现斑点状增强(中心性斑点区),肝脏周围区域增强不明显,并且出现门静脉广泛显影,提示门静脉血液离肝而去。注射造影剂后60s,肝内出现低密度带状影绕以边缘增强,或称之为肝静脉和下腔静脉充盈缺损,此种征象高度提示管腔内血栓形成,边缘增强是由于血管壁滋养血管显影所致。
在B-CS亚急性期或慢性期,CT平扫可见肝尾状叶明显增大,肝脏可有部分萎缩而另有部分代偿性肿大,在肝脏萎缩区或周边区,CT平扫呈低密度带,可能与静脉阻塞引起的病变,如淤血、出血坏死或纤维化有关。肝静脉不显影见于75%的病例,这多为B-CS的特征性表现。少数病例呈现肝静脉扩张或充盈缺损。由于肝静脉血流缓慢,在注射造影剂45~60s后,出现另一特征性改变,即斑点状影像。有时可见肝静脉侧支循环通路将血液由肝内引入右心房。Fishman认为CT对B-CS的诊断正确率为100%。
4.MRI显像 B-CS时MRI可显示肝实质的低强度信号,提示肝脏淤血,组织内自由水增加,MRI可清晰显示肝静脉和下腔静脉的开放状态,甚至可将血管内的新鲜血栓与机化血栓或瘤栓区分开来;MRI还可显示肝内侧支循环呈现的蛛网样变化,同时对肝外侧支循环亦可显示,因此可将MRI作为B-CS的非创伤性检查方法之一。
5.核素扫描 99mTc肝扫描对B-CS的诊断不具特异性,仅部分病例于尾状叶放射性吸收相对增加,但在鉴别海绵状肝血管瘤时有重要参考价值。
6.内镜检查 胃镜对B-CS的诊断帮助不大。但在慢性病例,特别是对曾有消化道出血者,可进一步了解出血原因、部位;对食管、胃底静脉曲张的程度、范围及相伴的食管、胃贲门部的炎症、糜烂等的了解,便于预测出血或再发出血,同时可对适宜的病例,进行内镜下的硬化剂注射和曲张静脉团的套扎等防治措施。腹腔镜检查,可见肝大、淤血,呈紫色或黑紫色。急性期肝表面光滑,可见滴状淋巴液自肝表面溢出;慢性期可见肝表面有粟粒状结节,或可见肝脏部分萎缩,但罕见大结节,与肝炎后肝硬化和亚急性重型肝炎所见不同,也与肝小静脉闭塞病和肝紫癜病有别。对可疑的或鉴别困难的病例,直视下取活检,更可明确诊断。腹腔镜下活检有更安全、可靠的优点。



 流行病学
流行病学
 病因
病因

 发病机制
发病机制
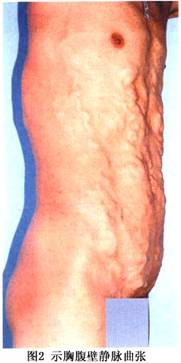
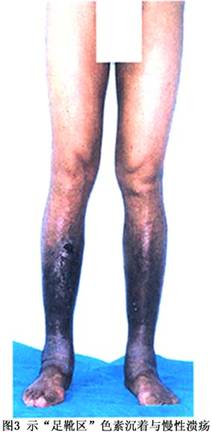
 临床表现
临床表现

 实验室检查
实验室检查
 其他辅助检查
其他辅助检查
 诊断
诊断
 鉴别诊断
鉴别诊断
 治疗
治疗
 预后
预后
 预防
预防